Quimica 11-9
Leyes de gases
Empecemos desde las primeras clases las cuales nos incursionamos en el tema de la química en saber cuales son las leyes que constituyen este tema que se dividen en 3.
-Ley de Gay Lussac: esta se define por al aumentar la temperatura de un gas las moléculas del gas se mueven mas rápidamente y por lo tanto aumenta el numero de choques contra las paredes. Es decir aumenta la presión ya que el recipiente es de paredes fijas y su volumen no puede cambiar.

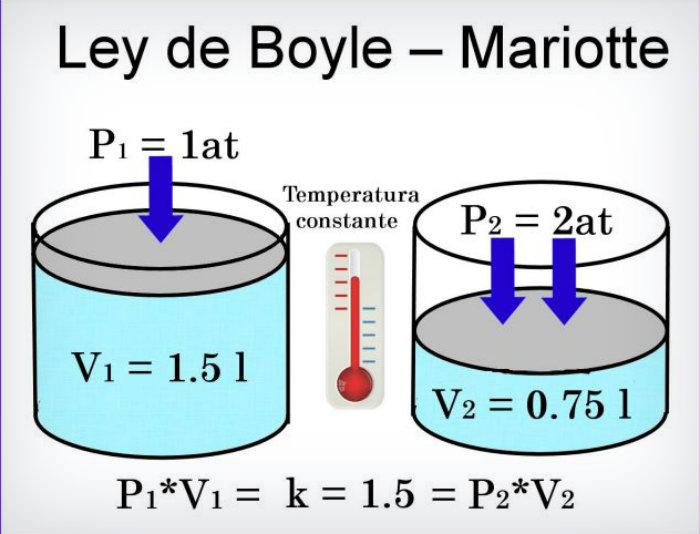
-Ley de Boyle: al aumentar el volumen, las partículas (átomos o moléculas) del gas tardan mas en llegar a las paredes del recipiente y por tanto chocan menos veces por unidad de tiempo contra ellas. Esto significa que la presión sera menor ya que esta representa la frecuencia de choques del gas contra las paredes.

-Ley de Charles: la ley de charles es una de las leyes de los gases. Relaciona el volumen y la temperatura de una cierta cantidad de gases ideal, mantenida a una presión constante, mediante una constante de proporcionalidad eléctrica.
En esta ley, jacques charles dice que para una cierta cantidad de gas es una constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura, el volumen del gas disminuye.
1).
En esta ley, jacques charles dice que para una cierta cantidad de gas es una constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura, el volumen del gas disminuye.
1).
2).

Como podemos solucionar estas leyes, lo veremos en las siguientes imagines tomadas del cuaderno de química que consta de todos los procedimientos.
-Ley de Boyle:












la información es muy concisa y detallada sobre el tema de las leyes.
ResponderEliminares un trabajo muy completo debido a que nos muestra gráficas, imágenes y formulas químicas para que tengamos mayor comprensión del tema
ResponderEliminarEsta muy bien explicado el tema esta muy bien explicado con las imágenes se puede hacer una mejor idea de este tema
ResponderEliminar